高一化学第二学期期末检测试卷
编辑:
2016-06-11
14.已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化
H2O2 → H2O IO3- →I MnO4- → Mn2+ HNO3 → NO
如果用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )。
A.H2O2 B.IO3- C.MnO4- D.HNO3
15.下列离子方程式书写正确的是( )。
A.向漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
B.氢氧化钠溶液中通入过量的二氧化硫:SO2+OH-=HSO3-
C.碳酸氢钙溶液中加足量的氢氧化钠溶液:Ca2++OH-+HCO3-==CaCO3↓+H2O
D.稀硫酸和氢氧化钡溶液:Ba2++SO42-==BaSO4↓
16.某温度时CuSO4的溶解度是25 g,若温度不变,将32 g 无水CuSO4粉末撤入m g 水中,形成饱和溶液并有CuSO4·5H2O晶体析出时,则m的取值范围是( )。
A.18 g≤m≤128 g B.36 g
17.由10 g 含有杂质的CaCO3和足量盐酸反应,产生了0.1 mol CO2,推断杂质的组成可能是( )。
A.KHCO3和MgCO3 B.K2CO3和Na2CO3
C.MgCO3和Na2CO3 D.Na2CO3和BaCO3
18.67 g 过氧化钠吸收二氧化碳后,其质量增加到72.6 g,则被吸收的二氧化碳的质量是( )。
A.4.4 g B.8.8 g C.11.0 g D.16.4 g
19.下列说法正确的是( )。
A.因为CO2通入水玻璃中可制取H2SiO3,说明H2CO3的酸性比H2SiO3强
B.因为SiO2和CaCO3固体混合加强热时,产生CO2气体,说明H2CO3的酸性比H2SiO3弱
C.SiO2既能溶于强碱溶液,又能和HF反应,故它是两性氧化物
D.因为玻璃中含SiO2,故玻璃试剂瓶不能盛装碱液
20.右图所示中,x表示通入气体的量,y表示溶液中H+的物质的量。下列反应中与图中变化关系相符合的是( )。
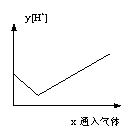
A.向饱和H2S溶液中通入过量的Cl2 B.向饱和H2S溶液中通入过量的SO2
C. 向饱和SO2溶液中通入过量的H2O D.向NaOH溶液中通入过量的Cl2
二、填空(共30分)
21、(4分)已知反应 8NH3 + 3Cl2 == 6NH4Cl + N2 ,若有42克N2 生成,则:
(1) 有 克NH3参加反应(2)被氧化的NH3 是 克。
22.(4分)实验室里盛放碱液的试剂瓶瓶塞不能用玻璃塞,是因为 (用离子反应方程式表示),检验生石灰里含有石英和石灰石的方法是 。
23.(4分)已知氧和硫、氧化物和硫化物在化学性质上具有相似性,用化学方程式分别表示下列变化。
⑴CS2与Na2S溶液一起振荡,溶液由无色变成有色:______________________________________________________
(2)Na2S2溶于足量稀盐酸中,产生浅黄色沉淀,并放出气体:
24.写出两个符合以下两个条件的置换反应①所涉及到的元素均为短周期元素②4种单质属于4个不同主族。______________________________________、__________________________
25、(9分)已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层的三倍,Y和Z可以形成两种以上的气态化合物。则:
(1)、X是_______Y是_______Z是_______(填元素符号)
(2)、由Y和Z组成,且Y和Z的质量比为7:20的化合物的化学式是_______。
(3)、由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子总数的两种离子是_______和_______。
(4)、X、Y、Z可以形成一种盐,此盐中X、Y、Z元素原子的个数比为4:2:3,该盐的化学式为_______。
26、(5分)用合适的试剂除去括号内的杂质。
(1)CO2(SO2)____________ (2)NaHCO3(Na2CO3) _____________
(3)FeCl3(FeCl2)_____________ (4)Fe2O3(Al2O3)_____________
(5)CO(CO2)_____________
三、实验题(11分)
27、用下图组装实验可以研究CO的还原性:
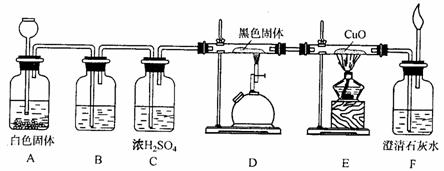
填写下列空白:
(1)从A的长颈漏斗应加入的试剂是______________(填编号)
A.稀硫酸 B.浓硫酸 C.稀盐酸 D.浓硝酸
(2)装置B中最适宜的试剂是_______ __。作用是_______ __。
(3)(2分)装置D中发生反应的化学方程式是________________________________。
(4)装置E中发生的现象是___________________________。
(5)(2分)必须用装置C吸收除去气体中水蒸气的理由主要是_____________________。
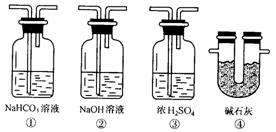
(6)若根据F中石灰水变浑浊的现象也能确认CO具有还原性,应在图中装置______________与______________之间连接下图的哪一种装置______________(填编号)。
四、计算题(9分)
28、 3.2克Cu与50 mL 浓硫酸H2SO4(足量)在加热的条件下充分反应。
(1)(2分)被还原的H2SO4物质的量为__________。
(2)(2分)若向50 mL 浓度为a mol/L 浓硫酸中投入足量的铜片加热,充分加热后,被还原的硫酸的物质的量n(H2SO4)__________0.025a mol(填“<”、“>”或“=”)
(3)(5分)把题干中反应后的溶液稀释至500 mL,取出50 mL,并向取出的溶液中加入足量的BaCl2 溶液中,得沉淀20.27 g,求原浓H2SO4的物质的量浓度?
相信大家在阅读了高一化学第二学期期末检测试卷之后,一定要及时漏题追踪,做好笔记哦。
相关推荐:
标签:高一化学试题
免责声明
精品学习网(51edu.com)在建设过程中引用了互联网上的一些信息资源并对有明确来源的信息注明了出处,版权归原作者及原网站所有,如果您对本站信息资源版权的归属问题存有异议,请您致信qinquan#51edu.com(将#换成@),我们会立即做出答复并及时解决。如果您认为本站有侵犯您权益的行为,请通知我们,我们一定根据实际情况及时处理。