嘉峪关2014年中考化学溶解度的曲线
编辑:sx_zhangby
2014-01-15
【摘要】中考作为重点高中招生的选拔性考试,日益受到学生的重视。为此精品学习网中考频道为大家提供中考化学溶解度的曲线,希望大家在复习的过程中有所参考!
溶解度
1、固体的溶解度
(1)溶解度定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量
四要素:①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:单位:克
(2)溶解度的含义:
20℃时NaCl的溶液度为36g含义:
在20℃时,在100克水中最多能溶解36克NaCl
或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克
(3)影响固体溶解度的因素:①溶质、溶剂的性质(种类) ②温度
a.大多数固体物的溶解度随温度升高而升高;如KNO3
b.少数固体物质的溶解度受温度的影响很小;如NaCl
c.极少数物质溶解度随温度升高而降低。如Ca(OH)2
(4)溶解度曲线
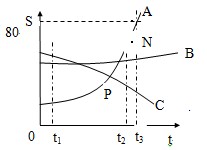
(1)t3℃时A的溶解度为 80g
(2)P点的的含义在该温度时,A和C的溶解度相同
(3)N点为 t3℃时A的不饱和溶液 ,可通过加入A物质,降温, 蒸发溶剂的方法使它变为饱和
(4)t1℃时A、B、C、溶解度由大到小的顺序C>B>A
(5)从A溶液中获取A晶体可用降温结晶的方法获取晶体。
(6)从A溶解度是 80g .
(7)t2℃ 时A、B、C的饱和溶液各W克,降温到t1℃
会析出晶体的有A和B 无晶体析出的有 C ,所得溶液中溶质的质量分数由小到大依次为 A
(8)除去A中的泥沙用过滤 法;分离A与B(含量少)的混合物,用结晶法
2、气体的溶解度
(1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)影响因素: ①气体的性质 ②温度(温度越高,气体溶解度越小)
③压强(压强越大,气体溶解度越大)
3、混合物的分离
(1)过滤法:分离可溶物 + 难溶物
(2)结晶法:分离几种可溶性物质
结晶的两种方法
a.蒸发溶剂,如NaCl(海水晒盐)
b.降低温度(冷却热的饱和溶液,如KNO3)
希望我们提供的中考化学溶解度的曲线在大家的复习过程中能够发挥真正的作用,能够帮助大家考入自己心目中理想的高中学校!
相关推荐
标签:嘉峪关中考化学
免责声明
精品学习网(51edu.com)在建设过程中引用了互联网上的一些信息资源并对有明确来源的信息注明了出处,版权归原作者及原网站所有,如果您对本站信息资源版权的归属问题存有异议,请您致信qinquan#51edu.com(将#换成@),我们会立即做出答复并及时解决。如果您认为本站有侵犯您权益的行为,请通知我们,我们一定根据实际情况及时处理。