2016学年高一化学《开发利用金属矿物和海水资源》达标测试
编辑:sx_yanxf
2016-05-25
在考试中能否取得好成绩不仅需要好的心态,还需要在考试中对于各种题型都能熟练应对,下面由精品学习网为大家整理了精编开发利用金属矿物和海水资源达标测试,供大家参考。
选择题
常言“真金不怕火炼”从化学的角度对这句话的理解正确的是( )
A.金的熔点高,难于熔化
B.金的化学性质稳定,不易变质
C.金越炼越纯
D.金的硬度大,高温下难于变形
从海水中提取镁的工艺流程可表示如下:
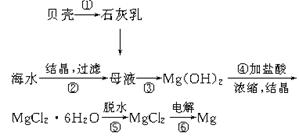
下列说法不正确的是( )
A.用此法提取镁的优点之一是原料来源丰富& h: P9 K/ W A1 U8 C
B.步骤⑥电解MgCl2时阴极产生氯气& h: P9 K/ W A1 U8 C
C.步骤⑤可将晶体置于HCl气体氛围中脱水& h: P9 K/ W A1 U8 C
D.上述工艺流程中涉及化合、分解和复分解反应& h: P9 K/ W A1 U8 C
海水提溴过程中将Br-氧化成Br2,可向其中加入氧化剂,合适的是( )
A.酸性KMnO4溶液& A" [7 g+ `9 f% Y1 L5 O* b B.氯水& A" [7 g+ `9 f% Y1 L5 O* b C.FeCl3溶液& A" [7 g+ `9 f% Y1 L5 O* b D.碘水& A" [7 g+ `9 f% Y1 L5 O* b
广东正在建设海洋强省。下列说法不正确的是( )
A.从海带中提取碘单质的过程涉及氧化还原反应0 I! f- [6 Q ?0 [7 O2 W4 S! N$ N* [
B.往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输0 I! f- [6 Q ?0 [7 O2 W4 S! N$ N* [
C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的0 I! f- [6 Q ?0 [7 O2 W4 S! N$ N* [
D.海洋经济专属区的资源开发可获得Fe、Co、K、Au、Mg等金属0 I! f- [6 Q ?0 [7 O2 W4 S! N$ N* [
下列说法不正确的是( )
A.海洋是一个远未完全开发的巨大化学资源宝库% b$ K: E7 W9 `' T! d; a
B.海水中金的储存量约为陆地的170倍,但它的富集程度却很低% b$ K: E7 W9 `' T! d; a
C.从海水中可以提取铀和重水等核原料% b$ K: E7 W9 `' T! d; a
D.海水中的溴、氟等元素均为微量元素,但仍有提取的价值% b$ K: E7 W9 `' T! d; a
NaCl是海水中提取出来的一种重要物质,除食用外,它还是一种工业原料,下列以NaCl为原料的产品(或物质)是( )
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸
A.①②③④⑤' i- L5 f' [ B.①②③④' i- L5 f' [ C.①②③⑤' i- L5 f' [ D.①②④⑤' i- L5 f' [
水资源非常重要,联合国确定2003年为国际淡水年。下列关于水的说法中错误的是( )
A.蒸馏法是海水淡化的方法之一
/ S9 H, Y/ O. J5 B7 a; H8 B
B.淡水的密度小于海水的密度
/ S9 H, Y/ O. J5 B7 a; H8 B
C.融化的雪水中矿物质含量比深井水中的少
/ S9 H, Y/ O. J5 B7 a; H8 B
D.0℃以上,温度越高,水的密度越小
/ S9 H, Y/ O. J5 B7 a; H8 B
下列各组元素中既包括海水中的常量元素,又包括海水中的微量元素的是( )
A.Cl、Na、C、F B.S、Ca、U、I
C.B、F、H、Sr D.Cl、Na、Li
铜在自然界多以+1价矿石存在,因为在固态特别是高温下+1价铜的化合物比+2价稳定。从辉铜矿(Cu2S)炼铜的方法之一是:①将矿石高温通空气焙烧,生成两种氧化物。②将焙烧过的矿石加上比它质量约少一半的未经焙烧过的矿石,混合后隔绝空气再进行高温燃烧,结果得到金属铜和一种具有刺激性气味的气体。写出这两个反应的化学方程式。
在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是( )
A.Mg. T4 [, R' e) j/ [ B.Cu. T4 [, R' e) j/ [ C.Ag. T4 [, R' e) j/ [ D.H2. T4 [, R' e) j/ [
已知工业上真空炼铷的反应方程式如下:2RbCl+Mg
![]()
MgCl2+2Rb(g),对此反应能够进行的正确解释是( )
A.铷比镁的金属性强( i& V$ K- H4 J$ C1 T! X* N
B.铷的沸点比镁低,把铷的蒸气抽走后,平衡向正反应方向移动( i& V$ K- H4 J$ C1 T! X* N
C.MgCl2的热稳定性比RbCl弱( i& V$ K- H4 J$ C1 T! X* N
D.高温下Mg2+得电子能力比Rb+弱( i& V$ K- H4 J$ C1 T! X* N
金属锂是密度最小的金属,等质量的金属,锂可以释放出更多的电子,故常用来制造高性能电池。已知锂的金属性介于钠和镁之间,则冶炼金属锂应采用的方法是( )
A.电解法+ f. K9 [. S6 Y$ f% [4 U" K; C B.热还原法+ f. K9 [. S6 Y$ f% [4 U" K; C C.热分解法+ f. K9 [. S6 Y$ f% [4 U" K; C D.铝热法+ f. K9 [. S6 Y$ f% [4 U" K; C
实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是( )
A.Fe2O3和MnO2
* K+ ^/ [6 G9 G/ A
B.MnO2和V2O5
* K+ ^/ [6 G9 G/ A
C.Cr2O3和V2O5
* K+ ^/ [6 G9 G/ A
D.Fe3O4和FeO
* K+ ^/ [6 G9 G/ A
下列各种冶炼方法中,可制得相应金属的是( )
A.加热分解氧化铝+ U/ j. c- T4 d% J0 F/ G, a8 e0 F B.高温下分解碳酸钙+ U/ j. c- T4 d% J0 F/ G, a8 e0 F
C.电解氯化钠溶液+ U/ j. c- T4 d% J0 F/ G, a8 e0 F D.三氧化钨与铝粉高温反应+ U/ j. c- T4 d% J0 F/ G, a8 e0 F
下列说法中正确的是( )
A有些活泼金属如铝可作高温还原法的还原剂
B.用电解NaCl溶液的方法来冶炼金属钠
C.可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝
D.回收旧金属可以重新制成金属或它们的化合物
热还原法冶炼金属的反应一定是( )
A.氧化还原反应- L- b% g' L' @ B.置换反应- L- b% g' L' @
C.复分解反应- L- b% g' L' @ D.分解反应- L- b% g' L' @
精品学习网给大家推荐的精编开发利用金属矿物和海水资源达标测试,大家仔细阅读了吗?祝大家在今后的学习中生活愉快。
相关推荐:
标签:高一化学同步练习
免责声明
精品学习网(51edu.com)在建设过程中引用了互联网上的一些信息资源并对有明确来源的信息注明了出处,版权归原作者及原网站所有,如果您对本站信息资源版权的归属问题存有异议,请您致信qinquan#51edu.com(将#换成@),我们会立即做出答复并及时解决。如果您认为本站有侵犯您权益的行为,请通知我们,我们一定根据实际情况及时处理。