高三化学选修3第三章晶体结构与性质单元测试题(人教版)
编辑:sx_gaohm
2016-10-14
化学如同物理一样皆为自然科学的基础科学。精品学习网为大家推荐了高三化学选修3第三章晶体结构与性质单元测试题,请大家仔细阅读,希望你喜欢。
1.科学家最近又发现了一种新能源——“可燃冰”。它的主要成分是甲烷分子的结晶水和物(CH4·nH2O)。其形成过程是:埋于海底地深处的大量有机质在缺氧环境中,厌氧型细菌把有机质分解,最后形成石油和天然气(石油气),其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”。这种“可燃冰”的晶体类型是( )。
A.离子晶体 B.分子晶体 C.原子晶体 D.金属晶体
2.下列各组物质汽化或熔化时,所克服的粒子间的作用力属于同种类型的是( )。
A.碘和干冰的升华 B.二氧化硅和生石灰的熔化
C.氯化钠和铁的熔化 D.苯和乙烷的蒸发
3.下列叙述中,错误的是( )。
A.离子化合物中可能含有非极性键 B.分子晶体中的分子内不含有离子键
C.原子晶体中可能含有非极性键 D.分子晶体中的分子内一定有共价键
4.下列各组物质中,按熔点由低到高排列正确的是( )。
A.O2、I2、Hg B.CO2、KCl、SiO2
C.Na、K、Rb D.SiC、NaCl、SO2
5.有下列物质①白磷 ②金刚石 ③石墨④二氧化硅 ⑤甲烷 ⑥四氯化碳 ⑦单质硅⑧铵离子,其分子结构或晶体结构单元中存在正四面体的是( )。
A.除③外 B.①②⑤⑥ C.除③⑧外 D.除③④⑦⑧
6.下列性质中,可以证明某化合物内一定存在离子键的是( )。
A.可溶于水 B.具有较高的熔点
C.水溶液能导电 D.熔融状态能导电
7.下面有关晶体的叙述中,不正确的是( )。
A.金刚石空间网状结构中,由共价键形成的碳原子环中,最小环上有6个碳原于
B.氯化钠晶体中,每个Na+周围距离相等的C1-共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻10个CO2分子
8.科学家最近发现一种由钛原子和碳原子构成的气态团簇分子,如图1所示:图中顶角和面心的原子都是钛原子,棱的中心和体心的原子都是碳原子该分子的化学式是( )。
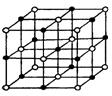
A.Til3C14 B.Ti14C13 C.Ti4C5 D.TiC
9.水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是 ( )
A.范德华力 B.共价键 C.氢键 D.相对分子质量
10.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )。
A.水由液态变为玻璃态,体积缩小 B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态 D.玻璃态水是分子晶体
11.20世纪80年代中期,科学家发现并证明碳还以新的单质形态C60存在。后来人们又相继得到了C70、C76、C84、C90、C94等另外一些球碳分子。90年代初,科学家又发现了管状碳分子和洋葱状碳分子。(如下图):下列说法错误的是( )。
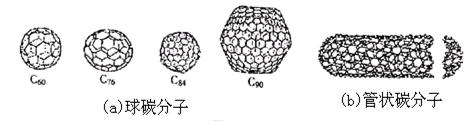
A.金刚石和石墨的熔点肯定要比C60高
B.据估计C60熔点比金刚石和石墨要高
C.无论是球碳分子,还是管状碳分子、洋葱状碳分子,都应看作是碳的同素异形体
D.球碳分子是碳的同素异形体,而管状碳分子、洋葱状碳分子则不一定
12.下列化学式既能表示物质的组成,又能表示物质分子式的是( )。
A.NH4NO3 B.SiO2 C.C6H5NO2 (硝基苯) D.Cu
13.2001年,日本科学家发现了便于应用、可把阻抗降为零的由硼和镁两种元素组成的超导材料。这是27年来首次更新了金属超导体的记录,是目前金属化合物超导体的最高温度。该化合物也因此被美国《科学》杂志评为2001年十大科技突破之一。图为该化合物的晶体结构单元示意图:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内。则该化合物的化学式可表示为( )。
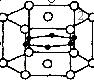
A.MgB B .MgB2 C.Mg2B D.Mg3B2
14.下列说法正确的是( )。
A.124 g P4含有的P-P键的个数为6NA
B.12 g石墨中含有的C-C键的个数为2NA
C.12 g金刚石中含有的C-C键的个数为1.5NA
D.60 g SiO2中含Si-O键的个数为2NA
15.下列物质中,既含极性键又含配位键的离子晶体是( )。
A.Ba(OH)2 B.H2SO4 C.(NH4)2SO4 D.CaF2
16.碳化硅这种结构类似于金刚石的晶体,其中碳原子和硅原子的位置是交替的。在下列三种晶体①金刚石 ②晶体硅 ③碳化硅中,它们的熔点从高到低的顺序是( )。
A.①③② B.②③① C.③①② D.②①③
17.实现下列变化,需克服相同类型作用力的是( )。
A.石墨和干冰的熔化 B.食盐和冰醋酸的熔化
C.液溴和水的汽化 D.纯碱和烧碱的熔化
18.下列表中给出几种氯化物的熔点和沸点:
|
晶体 |
NaCl |
MgCl2 |
AlCl3 |
Si Cl4 |
|
熔点(℃) |
810 |
710 |
180 |
-70 |
|
沸点(℃) |
1465 |
1418 |
177.8 |
57 |
据此,下列判断正确的是( )。
① 氯化铝加热时能升华②四氯化硅在室温下是液体③氯化钠在1500℃是以蒸汽形式存在④四氯化硅晶体是分子晶体
A. ②③ B.③④ C.①②③ D.①②③④
19.据报道,科研人员应用电子计算机模拟出类似C60的物质N60,试推测出该物质不可能具有的性质是 ( )
A.N60易溶于水 B.稳定性:N60
C.等物质的量时,分解吸收的热量:N60>N2 D.熔点:N60
20.组成晶体的质点(分子、原子、离子)以确定的位置在空间作有规则排列,具有一定几何形状的空间格子,称为晶格,晶格中能代表晶体结构特征的最小重复单位称为晶胞。在冰晶石(Na3AlF6)晶胞中,AlF63-占据的位置相当于NaCl晶胞中C1-占据的位置,则冰晶石晶胞中含有的原子数与食盐晶胞中含有的原子数之比为( )。
A.2:1 B.3:2 C.5:2 D.5:1
精品小编为大家提供的高三化学选修3第三章晶体结构与性质单元测试题,大家仔细阅读了吗?最后祝同学们学习进步。
相关推荐:
标签:高三化学试题
免责声明
精品学习网(51edu.com)在建设过程中引用了互联网上的一些信息资源并对有明确来源的信息注明了出处,版权归原作者及原网站所有,如果您对本站信息资源版权的归属问题存有异议,请您致信qinquan#51edu.com(将#换成@),我们会立即做出答复并及时解决。如果您认为本站有侵犯您权益的行为,请通知我们,我们一定根据实际情况及时处理。